近日,中国创新药出海再传捷报。远大医药集团自主研发的全球创新放射性核素偶联药物GPN01530,正式获得美国食品药品监督管理局批准,将开展用于诊断实体瘤的I/II期临床研究。这不仅意味着远大医药成功将其首款自研RDC产品推向全球监管最严格的市场,更标志着其在核药抗肿瘤诊疗领域的全球化战略,迈入了从引进合作至自主创新的全新阶段。
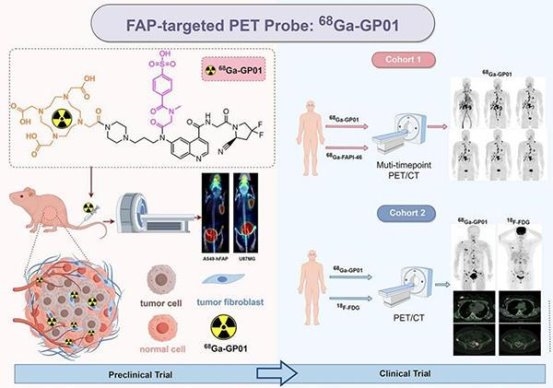
GPN01530是一款靶向成纤维细胞活化蛋白(FAP)的创新药物。研究表明,FAP在90%的上皮性肿瘤中高表达,是极具潜力的泛实体瘤靶点。相较于临床常用显像剂,靶向FAP的显像剂在胃癌、结直肠癌、肝癌等癌种中的检出灵敏度高达80%-90%。远大医药通过优化FAP配体结构,使GPN01530在早期研究中展现出更优的肿瘤靶向性和诊断效能,有望为实体瘤患者提供全新的精准诊断方案。
事实上,远大医药在核药抗肿瘤诊疗板块的布局早已超越单一产品维度,而是构建起覆盖研发、生产、销售的全产业链生态体系。在产品管线方面,公司围绕肿瘤诊疗一体化理念,在研发注册阶段已储备多款创新产品。这些产品涵盖多种放射性核素,覆盖了肝癌、前列腺癌、脑癌等在内的多个癌种。目前,公司已有数款创新RDC药物进入III期临床阶段,创新核药产品正逐步进入收获期。其中,用于治疗前列腺癌的全球创新RDC药物TLX591加入国际多中心III期临床试验的申请已获国家药监局默示许可。该研究将在全球多个国家和地区开展,旨在评估其对于特定前列腺癌患者的疗效和安全性。充分展现了远大医药为特定癌种提供全面诊疗解决方案的战略思维。

与此同时,集团已上市的核心产品持续释放临床与市场价值。其核药抗肿瘤诊疗板块的重磅产品易甘泰®钇[90Y]微球注射液在适应症拓展上接连取得突破性进展,先后获得美国FDA和欧洲CE认证,用于治疗不可切除的肝细胞癌(HCC),成为全球首个获批该双重适应症的选择性内放射治疗产品。随后,其在欧洲的适应症进一步扩展至肝内胆管癌等更广泛的肝脏恶性肿瘤,开启了“泛癌种治疗”的新阶段。临床数据显示,易甘泰®针对于不可切除HCC的客观缓解率高达98.5%;所有可评估患者均显示治疗反应,局部肿瘤控制率达到100%,为肝癌患者提供了全新的高效治疗选择。

远大医药集团核药抗肿瘤的硬核实力,背后是全产业链自主可控能力的强大支撑。公司位于成都的放射性药物全球研发及生产基地,已于2025年6月正式投入运营。该基地是全球首个“零辐射”智能核药工厂,拥有14条高标准GMP生产线,是目前国际范围内核素种类最全、自动化程度最高的智能工厂之一。这标志着远大医药成功搭建了覆盖“研发-生产-销售”的全产业链闭环,实现了从实验室创新到工业化量产的关键跨越,为包括抗肿瘤核药在内的自研创新产品生产提供了坚实保障。

如今,全球核药市场正迎来黄金发展期,已构建起丰富产品矩阵与全产业链优势的远大医药集团,正持续夯实其在中国乃至全球核药抗肿瘤诊疗领域的领军企业地位,为全球肿瘤患者带来更多精准诊疗新希望。














